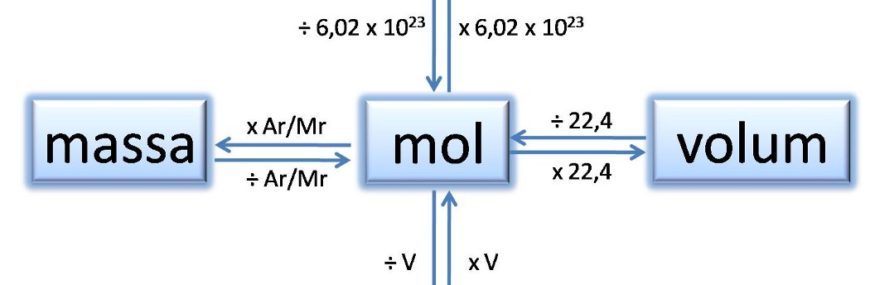
Hukum dasar kimia adalah hukum yang digunakan untuk mendasari hitung an kimia dan hubungan kuantitatif dari reaktan dan produk dalam persamaan kimia. Aspek kuantitatif dapat diperoleh dari pengukuran massa, volume, konsentrasi yang terkait dengan jumlah partikel atom, ion, molekul atau rumus kimia yang terkait dalam persamaan reaksi kimia.

Larutan dengan berbagai konsentrasi dan zat terlarut yang berbeda
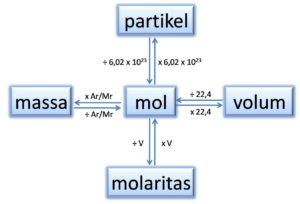
Skema pengubahan satuan jumlah
Pada perhitungan kimia secara stoikiometri memerlukan hukum-hukum dasar yang relevan. Ada beberapa hukum dasar yang penting diantaranya adalah
- Hukum kekalan massa (Hukum Lavoisier)
Antoine Laurent Lavoisier ilmuan yang melalukan mengamati percobaan dan mengungkapkan bahwa massa total zat sebelum reaksi akan selalu sama dengan massa zat hasil reaksi

Antoni Laurent Lavoisier
Contoh 1:Sebanyak 6 gram oksigen bereaksi tepat habis dengan 4 gram logam magnesium membentuk senyawa magnesium oksida. Berapakah massa nagnesium oksida yang dihasilkan?
massa zat sebelum reaksi = massa zat sesudah reaksi
massa magnesium oksida = massa oksigen + massa logam magnesium
10 gram massa magnesium = 6 gram massa oksigen + 4 gram massa logam magnesium
Contoh 2: Sebanyak 4,0 gram cuplikan yang mengandung senyawa hidrokarbon dibakar sempurna dengan gas oksigen. Jika presentase (%) massa karbon dalam cuplikan tersebut adalah 30%, maka massa karbon dioksida yang dihasilkan dalam proses pembakaran tersebut adalah…. (Ar C = 12, O = 16) maka hasil proses pembakaran dapat dihitung dengan cara menghitung massa karbon sebelum reaksi adalah:

Hasil hitungan massa atom karbon sebelum reaksi
dengan asumsi bahwa massa atom karbon sebelum reaksi dan sesudah reaksi sama maka massa atom karbon sebelum reaksi sama dengan massa atom karbon dalam senyawa CO2 sebagai hasil reaksi
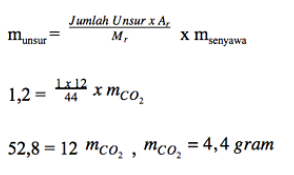
Massa CO2 setelah hasil reaksi
2. Hukum perbandingan tetap (Hukum Proust)
Joseph Louis Proust seorang ilmuan mengemukakan sifat penting dari senyawa yaitu perbandingan massa unsur dalam satu senyawa adalah tertentu dan tetap. Senyawa yang sama dari mana pun asalnya akan memiliki perbandingan massa unsur yang sama.

Joseph Louis Proust
Contoh: air memiliki rumus kimia H2O perbandingan massa hidrogen dan oksigennya dalam air H:O = 2 : 16 dapat disederhanakan 1:8 Dimanapun air berasal maka perbandingannya adalah sama yaitu antara hidrogen dan oksigennya 1:8
3. Hukum kelipatan perbandingan (Hukum Dalton)
John Dalton mengemukakan jika dua unsur membentuk lebih dari satu senyawa, dan jika massa salah satu unsur menyusunnya tetap, maka perbandingan massa unsur yang lainnya dalam senyawa tersebut merupakan bilangan bulat dan sederhana. Contoh unsur yang dapat membentuk lebih dari satu senyawa adalah CO dan CO2, PCl3 dan PCl5, N2O, NO, NO2, N2O5 dan lain sebagainya.

John Dalton
Contoh: Bila unsur nitrogen dan oksigen di senyawakan dapat terbentuk
NO dimana massa N : O = 14 : 16 = 7 : 8
NO2 dimana massa N : O =14 : 32 = 7 :16
Jika massa nitrogen yang sama banyaknya maka perbandingan massa oksigen pada senyawa NO : NO2 = 16 : 32 = 1 : 2
4. Hukum Perbandingan volume (Hukum Gay-Lussac)
Joseph Louis Gay Lussac mendasar pada hasil percobaannya mengemukakan bahwa volume gas-gas yang bereaksi dan volume gas-gas hasil reaksi bila diukur pada suhu dan tekanan yang sama berbanding sebagai bilangan bulat dan sederhana.

Joseph Louis Gay Lussac
Percobaan sederhana yang dilakukan menghasilkan perbandingan volume hidrogen : oksigen : uap air adalah 2 : 1 : 2. Nampak bahwa perbandingan volume sesuai dengan perbandingan koefisien unsur atau senyawa pada persamaan reaksi setara, yaitu persamaan reaksi dengan jumlah atom di sebelah kiri sama dengan di sebelah kanan.
Reaksi pembentukan air: 2H2 + O2 → 2H2O
volume gas hidrogen : Oksigen : uap air = 2 : 1 : 2
Contoh: N2(g) + H2(g) ⇌ NH3(g) Pada suhu dan tekanan yang sama, perbandingan volume gas-gas yang terlibat dalam reaksi tersebut secara berurutan adalah…
Berdasarkan Hukum Gay Lussac, pada suhu dan tekanan yang sama, volume gas-gas yang terlibat dalam reaksi sebanding dengan koefisien dalam reaksi tersebut.
Reaksi pembentukan amonia setelah setara adalah sebagai berikut:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Sehingga perbandingan volume gas N2, H2 dan NH3 berturut- turut adalah 1 : 3 : 2
5. Hipotesa Avogadro
Amadeo Avogadro mengungkapan hasil penelitiannya dengan kesimpulan jika gas-gas yang volumenya sama jika diukur pada suhu dan tekanan yang sama akan memiliki jumlah molul yang sama

Amadeo Avogadro
Contoh : Pada reaksi pembentukan air
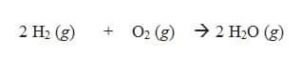
Reaksi pembentukan air
Jika volume gas H2 yang diukur pada suhu 25°C dan tekanan 1 atm sebanyak 10 L volume gas O2 dan H2O pada tekanan dan suhu yang sama dapat ditentukan dengan cara sebagai berikut.

Jika gas oksigen memiliki jumlah molekul sebanyak x maka uap air akan memiliki jumlah molekul sebanyak 2x